ACOBIOM présente les bénéfices cliniques du GemciTest® à l’ASCO 2021

Le texte présenté à la conférence annuelle de l’ASCO 2021 est une synthèse de l’étude des performances cliniques du test moléculaire IVD marqué CE afin d’évaluer la réponse à la gemcitabine dans le cancer du pancréas avancé.
L’adénocarcinome canalaire pancréatique (PDAC) est hautement létal et se présente souvent à un stade avancé. La gemcitabine reste un composant important du traitement du PDAC, bien qu’il n’existe pas de biomarqueur de routine permettant de prédire son efficacité. Dans une étude clinique précédente, ACOBIOM a identifié deux signatures ARN distinctes présentes dans le sang chez 60 patients montrant une association avec la survie sans progression (PFS) et la survie globale (OS). A partir de ces deux signatures ARN « sanguines », la société a développé le GemciTest®. Ce test moléculaire marqué CE nécessite un échantillon de 2,5 ml de sang total avant de commencer la chimiothérapie de première ligne du patient. A partir de cette biopsie liquide, ce Diagnostic In-Vitro mesure les niveaux d’expression de neuf gènes en utilisant des procédés standards de PCR en temps réel.
Dans cette étude, des validations cliniques ont été effectuées sur 214 patients (moyenne : 68,7 ans ; 37-88) provenant de 3 cohortes distinctes avec la Biobanque de l’Université du Wisconsin, l’essai clinique GemciPANC (NCT03599154), et la base clinico-biologique BACAP (NCT02818829). Ces cohortes comprenaient un traitement de première ligne avec un régime à base de gemcitabine ou de fluoropyrimidine.
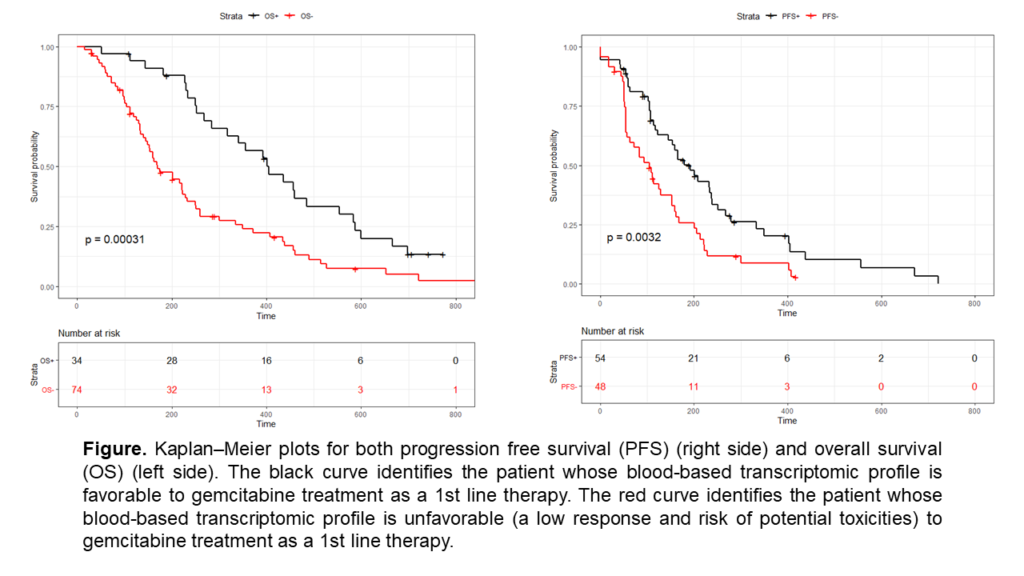
Les résultats de l’étude montrent que les patients présentant une réponse clinique bénéfique et identifiés par le GemciTest® (31,5 %) ont eu une survie sans progression (PFS) significativement plus longue (5,4 mois contre 3,1 mois, p = 0,0032) et une survie globale (OS) plus longue (13,1 mois contre 5,4, p < 0,0003). Dans les analyses multivariées incluant la localisation de la tumeur et le statut de performance, la signature GemciTest® a continué d’être associée à la PFS (HR = 0,52 (0,34-0,81) p = 0,003) et à la OS (HR = 0,44 (0,28-0,69) p = 0,0002).
Ce texte a été publié avec le soutien du Dr Noelle LoConte (Université du Wisconsin, Carbone Cancer Center, USA), du Dr Jérôme Cros (APHP, Paris, France), du Pr Barbara Bournet (BACAP, CHU de Toulouse, France) et du Pr François Ghiringhelli (essai clinique GemciPANC, CGFL – Centre Georges-François Leclerc, Dijon, France).
A propos de la collaboration ACOBIOM-UWCCC
Depuis 2018, ACOBIOM et le Carbone Cancer Center de l’Université du Wisconsin (UWCCC, Madison, Wisconsin, USA) collaborent avec l’objectif de développer une approche de médecine de précision dans le domaine du traitement de l’adénocarcinome pancréatique. Ce partenariat permettra le développement et la validation clinique de tests sanguins de diagnostic prédictif permettant d’identifier les patients les plus susceptibles de bénéficier des différents traitements. Ces tests sanguins visent à aider les médecins à prendre des décisions et à ajuster les pratiques de traitement dans le cancer du pancréas.
A propos de la collaboration ACOBIOM-BACAP
En 2018, ACOBIOM et le Centre Hospitalier de Toulouse ont signé un partenariat de 2 ans pour donner à l’entreprise l’autorisation durant d’avoir accès à la base de données BACAP, un programme clinique et biologique qui vise à rassembler dans une seule base de données : les données cliniques et épidémiologiques, ainsi que les échantillons biologiques associés, collectés auprès de patients atteints de cancer du pancréas. Ces patients atteints de cancer du pancréas seront recrutés par les différents centres cliniques partenaires de ce programme. Accordé par l’INCa et validé par les différentes autorités réglementaires françaises (CCTIRS, CNIL, CPP, autorisation de prélèvement obtenue auprès du ministère de la Santé), le programme BACAP recrute les patients (plus de 1000 à ce jour) ayant donné leur consentement éclairé.
A propos de l’étude clinique multicentrique GemciPANC
En 2018, le CGFL (Centre Georges-François Leclerc, Dijon, France) a lancé une étude exploratoire pour évaluer le Gemcitest™ chez des patients atteints de cancer du pancréas traités par chimiothérapie. L’objectif de cet essai clinique multicentrique est d’évaluer la valeur pronostique du Gemcitest™ chez les patients diagnostiqués avec un cancer du pancréas, opérable ou non, métastatique ou non. Pour évaluer ce test moléculaire sanguin, des échantillons de sang ont été prélevés chez les patients avant l’administration de la chimiothérapie de première ligne. Les patients ont été suivis selon les procédures standard des centres français pour leur pathologie.

